Eletroquímica é a parte da Físico-Química responsável por estudar os fenômenos de transformação de energia química em energia elétrica, bem como o processo inverso, e também estuda as reações em que há transferência de elétrons.
No caderno de Ciências da Natureza e suas tecnologias do ENEM, as questões de Química sempre são motivo de preocupação dos estudantes. Dentro dessa matéria, entender o que é Eletroquímica é essencial para responder questões que surgem sobre o tema.
Não deixe de conferir os exercícios sobre eletroquímica.
Nesse artigo vamos falar sobre:
- O que é Eletroquímica;
- Reações de Oxirredução;
- Pilhas e Eletrólise.
O que é Eletroquímica?
Eletroquímica é o ramo da Físico-Química que tem como objetivo estudar as reações em que ocorre a transferência de elétrons, bem como a transformação de energia química em energia elétrica e vice-versa.
Existem muitas reações químicas que ocorrem naturalmente e que liberam energia elétrica, e muitas dessas reações são utilizadas em baterias e células de combustível para gerar energia elétrica. Por outro lado, existem muitas correntes elétricas que podem ser usadas para ocasionar diversas reações químicas que não ocorrem de maneira espontânea. Mais à frente, iremos estudar cada um desses casos.
Conceitos Importantes
Energia Química
Energia química é a energia que se encontra armazenada em todas as matérias que possuem ligações químicas, sendo liberada a partir da quebra dessas ligações.
A energia química também pode ser apontada como uma energia potencial, visto que ela se encontra contida em determinadas matérias. Para que a energia química seja liberada, é preciso que aconteça uma grande interferência sobre a matéria, alterando a condição de suas ligações químicas.
Energia Elétrica
É a energia obtida através de cargas elétricas das partículas subatômicas. Ao se deslocarem, as cargas geram corrente elétrica, criando o que pode ser chamado de eletricidade.
Células Eletroquímicas
São células que produzem energia elétrica a partir de energia química. Essas células são a base de baterias e células de combustível.
Reação Eletroquímica
Reações eletroquímicas são processos causados ou acompanhados por passagens de corrente elétrica, e abrangendo a transferência de elétrons entre duas substâncias.
Muitas reações químicas são acompanhadas pela liberação ou pela absorção de calor. No entanto, muitas reações químicas, quando entram em contato com condutores elétricos, liberam a energia elétrica.
Condutores
Substâncias que são bons condutores de eletricidade podem ser classificadas em dois grupos:
- Metais: A passagem da corrente elétrica através deles produz aquecimentos e efeitos magnéticos, mas sem alterações químicas;
- Condutores eletrolíticos (Eletrólitos): compreendem a maior parte dos ácidos, bases e sais que têm a capacidade de conduzir correntes elétricas devido à presença de átomos eletricamente carregados ou grupos de átomos produzidos pela separação natural ou dissociação das moléculas da substância.
Reações de Oxirredução
Na eletroquímica estuda-se as reações de oxirredução, que são caracterizadas pela perda e ganho de elétrons. Ou seja, ocorre transferência de elétrons de uma espécie para outra. As reações de oxirredução ocorrem em duas etapas:
- Oxidação: Ocorre a perda de elétrons. O elemento que provoca oxidação é chamado de agente oxidante.
- Redução: Ocorre o ganho de elétrons. O elemento que provoca a redução é chamado de agente redutor.
É importante conhecer o número de oxidação dos elementos, para saber quem ganha e quem perde elétrons. Exemplo:
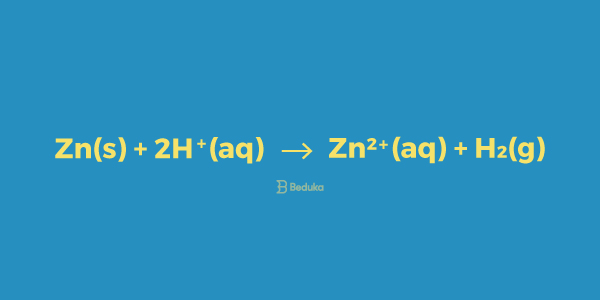
O elemento zinco (Zn2+) sofre a oxidação, pois ele perde dois elétrons. Ele também ocasionou a redução do íon de hidrogênio, por esse motivo, ele é chamado de agente redutor.
O íon (H+) sofre redução, pois ganha um elétron. Por isso ele provoca a oxidação do zinco e é chamado de agente oxidante.
Pilhas e Eletrólise
As pilhas e a eletrólise estão dentro dos estudos da eletroquímica. A diferença entre os dois é a transformação de energia.
- A pilha converte energia química em energia elétrica, de maneira espontânea;
- A eletrólise converte energia elétrica em energia química, de maneira não espontânea.
Pilhas

A pilha, também chamada de célula eletroquímica, é um sistema onde ocorre a reação de oxirredução. Ela é composta por dois eletrodos e por um eletrólito. Estes elementos, em conjunto, produzem energia elétrica. Quando conectamos duas ou mais pilhas, elas se tornam uma bateria.
O eletrodo é a superfície sólida condutora que possibilita a troca de elétrons.
- O eletrodo no qual ocorre a oxidação é chamado de ânodo, representa o pólo negativo da pilha;
- O eletrodo no qual ocorre a redução é catodo, o polo positivo da pilha.
Os elétrons são liberados no ânodo e seguem por um fio condutor até o catodo, onde ocorre a redução. Assim, o fluxo de elétrons segue de ânodo para o catodo.
O eletrólito ou ponte salina é a solução eletrolítica condutora dos elétrons, permitindo a sua circulação no sistema.
Eletrólise
A eletrólise é a reação de oxirredução que acontece de maneira não espontânea, provocada pela passagem de corrente elétrica vinda de fonte externa. A eletrólise pode ser ígnea ou aquosa.
- A eletrólise ígnea é aquela que se processa a partir de um eletrólito fundido, ou seja, pelo processo de fusão.
- Na eletrólise aquosa, o solvente ionizante utilizado é a água. Em solução aquosa, a eletrólise pode ser realizada com eletrodos inertes ou eletrodos ativos (ou reativos).
Aplicações da Eletroquímica
Podemos notar a eletroquímica em diversos aspectos do nosso cotidiano, como por exemplo:
- Reações no corpo humano;
- Fabricação de diversos aparelhos eletrônicos;
- Carregamento de baterias;
- Galvanoplastia: revestimento de peças de ferro e aço com zinco metálico;
- Diversos tipos de aplicação na indústria química.
Além de aprender o que é Eletroquímica, você pode testar seus conhecimentos e de outras matérias respondendo algumas questões que caíram em edições antigas do Exame em nosso simulado gratuito.
Gostou de aprender o que é Eletroquímica? Queremos te ajudar também a encontrar a FACULDADE IDEAL! Logo abaixo, faça uma pesquisa por curso e cidade que te mostraremos todas as faculdades que podem te atender. Informamos a nota de corte, valor de mensalidade, nota do MEC, avaliação dos alunos, modalidades de ensino e muito mais.
Experimente agora!





