Os elementos químicos são organizados na tabela periódica de acordo com seu número atômico e sua quantidade de prótons. Compreender como ler a tabela periódica é imprescindível quando estudamos Química, por esta razão preparamos este artigo completo sobre o assunto!
Se você quiser ir diretamente para alguma parte do texto, clique em um dos tópicos abaixo:
- O que é a Tabela Periódica?
- Como ler a Tabela Periódica?
- O que são as Propriedades Periódicas?
- Nós conectamos você à faculdade!
Estudando Química para o Enem? Depois de aprender como ler a tabela periódica, teste seus conhecimentos com o Simulado Beduka do Enem. Ele é totalmente gratuito e personalizável, acesse agora!
O que é a Tabela Periódica?
Antes de aprender como ler a tabela periódica, é interessante que você saiba do que se trata essa ferramenta e como ela funciona.
Basicamente, a tabela periódica é um modelo que organiza todos os elementos químicos existentes de forma sistematizada, de acordo com suas propriedades periódicas.
O número de prótons de um átomo (número atômico) e a disposição dos seus elétrons (configuração eletrônica) são responsáveis por determinar a posição de cada elemento na tabela.
A tabela periódica mais atual apresenta 118 elementos químicos, sendo 92 encontrados na natureza e 26 artificiais (sintetizados em laboratório).
- Quer saber mais sobre o assunto? Temos um artigo completo sobre os elementos da tabela periódica!
Depois de compreender o que é e sua importância para a Química, vamos para o que interessa: entender como ler a tabela periódica!
Como ler a Tabela Periódica?
Para facilitar seu entendimento de como ler a tabela periódica, elaboramos 7 dicas para você aprender a decifrar essa ferramenta completamente; acompanhe!
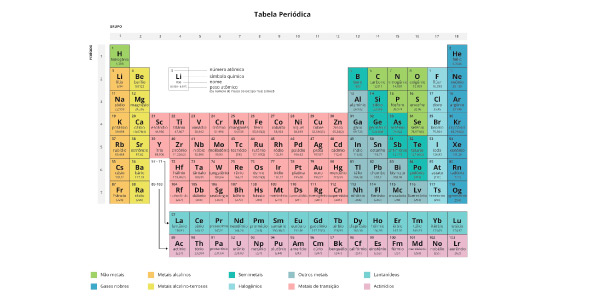
1. Comece a ler do canto superior esquerdo ao inferior direito
Com uma tabela periódica em mãos, observe a maneira como os elementos são distribuídos: linhas, colunas, cores, símbolos, nomes dos elementos e números.
Note que a distribuição segue uma sequência numérica (acima de cada elemento), assim a tabela deve ser lida do canto superior esquerdo ao inferior direito.
Obter essa visão ampla é um bom começo para interpretar a tabela periódica.
2. Perceba como o número atômico aumenta
A segunda dica é observar que essa sequência numérica aumenta a cada sucessivo elemento da tabela.
Esse número é denominado de número atômico e corresponde ao número de prótons que cada átomo possui em seu núcleo.
Algumas tabelas também apresentam uma numeração abaixo do símbolo do elemento; esse número é sua massa atômica e ela também aumenta da mesma forma que o número atômico, já que ela é a soma dos prótons e dos nêutrons de cada átomo.
3. Entenda o que são os grupos da tabela periódica
Os grupos da tabela periódica, também chamados de famílias, possuem propriedades físicas e químicas semelhantes e ficam nas colunas. Na maioria dos casos, possuem a mesma cor.
Cada membro de um grupo particular tem o mesmo número de elétrons na camada de valência.
Em geral, as colunas são numeradas de 1 a 18 e o número vem acima ou abaixo da tabela. Além disso, eles podem ser representados por algarismos romanos (IA), algarismos hindu-arábicos (1A) ou algarismos simples (1).
4. Aprenda o que são os períodos da tabela periódica
Os períodos são as linhas da tabela periódica.Todos os elementos em um período têm o mesmo número de camadas eletrônicas, onde estão contidos os elétrons.
O número de camadas em um átomo corresponde ao número do período. Ao todo existem sete camadas, dessa forma a tabela periódica contém sete períodos.
Está gostando desse tutorial de como ler a tabela periódica? Continue lendo pois temos mais 3 dicas importantes!
5. Observe as lacunas existentes na tabela
Apesar dos elementos serem distribuídos de acordo com o número atômico, eles também são classificados em grupos e famílias com propriedades físico-químicas semelhantes. E isso torna mais fácil entender seu comportamento.
Contudo, alguns elementos nem sempre se encaixam perfeitamente em determinados grupos e, por este motivo, a tabela periódica apresenta lacunas.
Por exemplo, as três primeiras linhas têm espaços em branco pois os metais de transição não aparecem na tabela até o valor do número atômico 21.
Além disso, os elementos 57 a 71, que são os lantanídeos, são mostrados como um pequeno grupo na parte inferior direita da tabela.
6. Diferencie os metais, semimetais e ametais
É fácil entender as propriedades dos elementos químicos quando entendemos sua natureza. Felizmente, a maioria das tabelas periódicas utiliza cores para separar tudo.
Os metais estão à esquerda, os não metais estão à direita e os semimetais estão no meio.
As características dos metais são:
- são sólidos à temperatura ambiente;
- conduzem calor e eletricidade;
- são atraentes e absorventes.
Já os elementos ametais:
- não brilham;
- não conduzem calor ou eletricidade;
- não são maleáveis.
- geralmente são gases à temperatura ambiente, embora possam ser sólidos ou líquidos sob certas condições.
Por fim, os elementos semimetais possuem características tanto dos metais como dos ametais.
7. Identifique os elementos e suas características
Os elementos são representados por uma ou duas letras e geralmente aparecem no centro de cada tabela, com fontes maiores. O símbolo abrevia o nome de um elemento da maneira usual e é o mesmo para qualquer idioma.
Por sua vez, o número atômico é escrito acima de cada elemento, no meio ou no canto. Os números são consecutivos e variam de 1 a 118. Ele sempre será um número inteiro, nunca um decimal.
- Agora que você já sabe como ler a tabela períodica, que tal testar o que aprendeu com os 18 melhores exercícios sobre o assunto?
O que são as propriedades periódicas?
Há também como ler a tabela periódica de outras maneiras, mais especificamente, por meio das propriedades periódicas.
As propriedades periódicas dos elementos químicos são certas características que variam em intervalos regulares, de acordo com o aumento ou a diminuição dos números atômicos.
Entenda a seguir como ler a tabela periódica através das principais propriedades:
Raio atômico: é a metade da distância (r = d/2) entre os núcleos de dois átomos de um mesmo elemento químico, considerando os átomos como esferas e sem estarem ligados.
Na tabela periódica, o raio atômico aumenta de cima para baixo e da direita para esquerda.
Energia de ionização: é a energia mínima necessária para retirar um elétron da última camada eletrônica de um átomo ou íon no estado gasoso.
É contrária ao raio atômico, aumentando de baixo para cima e da esquerda para direita na tabela periódica.
Eletronegatividade: é a capacidade que um átomo tem de atrair elétrons para si, em uma ligação química de uma molécula isolada. Ela aumenta de baixo para cima e da esquerda para a direita na tabela periódica.
Eletropositividade: é a tendência que um átomo possui de se afastar de seus elétrons mais externos, em comparação com outro átomo, na formação de uma substância composta.É oposta à eletronegatividade, aumentando de cima para baixo e da direita para a esquerda.
Afinidade eletrônica: é a energia liberada por um átomo do estado gasoso, quando um elétron é capturado. Essa energia possui este nome, pois mostra um grau de afinidade da atração do elétron adicionado.
Nem todos os elementos apresentam valores de eletroafinidade, mas os que têm, possuem um padrão de aumento de baixo para cima e da esquerda para a direita na tabela periódica.
- Você sabe qual é o primeiro elemento da tabela periódica? Descubra essa e outras curiosidades aqui!
Esperamos que este artigo sobre como ler a Tabela Periódica tenha despertado em você a vontade de estudar mais sobre o fantástico mundo da Química!
Logo abaixo temos uma oportunidade incrível para você, não deixe de conferir!
Nós conectamos você à faculdade!
Você sabia que é possível entrar na faculdade sem fazer o Enem? Sim! E o melhor, você pode realizar seu sonho e ainda economizar dinheiro.
Conheça o Beduka Bolsas, a plataforma do Beduka disponível 24 horas, onde você pode encontrar bolsas de estudo com até 65% da mensalidade!
Faça a faculdade dos seus sonhos, escolhendo entre mais de 90 opções de cursos em uma de nossas universidades parceiras.
Siga também o Beduka nas redes sociais! Em nosso Instagram você encontra todos os conteúdos que podem cair no Enem e no Pinterest os melhores resumos sobre todas as matérias cobradas no vestibular.
É tudo gratuito e pensado em te ajudar a entrar na faculdade!
Obrigada por ler nosso resumo sobre como ler a tabela periódica.





