O que é Equilíbrio Iônico? É o estudo do equilíbrio químico de ácidos e bases em soluções aquosas, além de moléculas não ionizadas. Esta grandeza indica quanto por cento do ácido sofreu ionização, indicando a força do ácido ou da base.
Você já ouviu falar em Equilíbrio Iônico? O Beduka preparou esse artigo para você entender melhor sobre esse tema e se preparar melhor para a prova de química do ENEM e de outros vestibulares.
Não deixe de conferir nossos Exercícios de Equilíbrio Iônico!
Nesse artigo vamos falar sobre:
- O que são Íons;
- O que é Ionização;
- O que é Equilíbrio Iônico.
O que são Íons?
Íons são átomos que possuem carências ou excesso de elétrons. Quando os átomos perdem ou ganham elétrons, eles deixam de ser neutros e passam possuir uma carga elétrica, e recebem o nome de íons.
Quando o átomo recebe uma carga positiva, ou seja, quando ele perde um elétron, este íon é chamado de cátion. Quando o átomo recebe uma carga negativa, ou seja, quando ele ganha um elétron, este íon é chamado de ânion.
Mesmo sendo carregados eletricamente, alguns íons podem ser mais estáveis que alguns átomos neutros. Por exemplo, o íon fluoreto (F–) é um átomo de flúor que ganhou um elétron, ou seja, assumiu uma carga negativa. Entretanto, a adição desse elétron faz com que a camada de valência (última camada eletrônica) possua 8 elétrons, adquirindo mais estabilidade.
O que é Ionização?
A ionização é o processo onde os átomos ou um grupo de átomos neutros são carregados eletricamente, ou seja, se transformam em íons. O processo de ionização pode ocorrer em inúmeras situações, seja em meios líquidos, sólidos ou gasosos.
A ionização diz respeito a uma reação entre compostos moleculares, produzindo íons que não existiam antes. Por exemplo, em uma solução líquida em que moléculas neutras de HCl reagem com moléculas de H2O, elas produzem os íons H3O+ e Cl–.
Isso acontece devido ao Cl receber o elétron por ser o elemento mais eletronegativo, isto é, ele apresenta tendência a ganhar elétrons. Podemos observar o processo de ionização na equação:
HCl(aq) + H2O(l) → H3O+(aq) + Cl–(aq)
Esse processo também pode acontecer por radiação, quando uma grande quantidade de energia emitida é suficiente para fazer com que, durante a interação com o átomo ou molécula, os elétrons se energizem até o ponto em que se desprendem de sua órbitas, fazendo com que o átomo seja ionizado.
Dissociação Iônica
A dissociação iônica é a separação de íons que ocorre a partir de compostos iônicos dissolvidos em água. A água interage com os íons e provoca a sua separação, um fenômeno denominado de solvatação. Quando o NaCl é colocado em água, temos a seguinte equação:
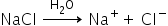
O NaCl é um composto iônico, por isso os íons já existiam, o que ocorreu foi apenas a separação entre eles através da ação da água.
Ácidos e bases
Ácidos são compostos covalentes, isto é, realizam o compartilhamento de elétrons em suas ligações. Eles são capazes se sofrer o processo de ionização quando em contato com a água. Quando isso acontece, os ácidos formam cargas, liberando o H+ como único cátion.
Bases são compostos iônicos formados por um metal, e que possuem a capacidade de sofrer o processo de dissociação quando em contato com a água. Quando isso acontece, as cargas são separadas, liberando o OH- como único ânion.
Aprenda mais sobre as funções inorgânicas da química.
Equilíbrio Químico
Para entender sobre Equilíbrio Iônico, precisamos entender primeiro o que é equilíbrio químico. É o nome dado ao processo dinâmico em que as quantidades de reagentes e produtos sempre se mantém constantes, e a velocidade dessas reações são as mesmas. Em um sistema fechado, a reação química engloba dois processos de reação:
- Reação direta: os reagentes são convertidos em produtos;
- Reação inversa ou reversa: os produtos são convertidos em reagentes

A e B são os reagentes
C e D são os produtos
V1 = Velocidade da reação direta
V2 = Velocidade da Reação inversa
Quando o equilíbrio químico é atingido, as velocidades da reação direta e indireta são as mesmas, existindo no sistema reagentes e produtos ao mesmo tempo. As reações não param de acontecer em momento algum, somente suas velocidades são igualadas.
Confira o artigo completo sobre o que é Equilíbrio Químico.
Equilíbrio Iônico
Os ácidos são compostos covalentes que reagem com a água e sofrem ionização, ou seja, íons que não existiam são formados, apresentando o cátion H+. As bases, como vimos, são compostos que sofrem dissociação na água, isto é, íons que já existiam são separados, liberando o ânion OH-.
Essas reações de ionização e dissociação são reações reversíveis, ou seja, que podem ocorrer de forma direta ou inversa. Por ser reversíveis, essas reações podem alcançar o equilíbrio químico. Considerando o ácido HCl e a base NaOH, em contato com a água temos as reações:
HCl ↔ H+ + Cl–
e
NaOH ↔ Na+ + OH–
Entretanto, nem sempre todas as moléculas dos ácidos e das bases sofrem ionização e dissociação ao entrar em contato com a água, geralmente, somente uma parte dessas moléculas sofrem esses processos.
Por isso, pode-se dizer que cada ácido e cada base possui um grau de ionização, que determina a porcentagem das moléculas que foram ionizadas ou dissociadas na água. Pode-se definir o grau de ionização através da fórmula:

Onde α representa o grau de ionização
O ácido clorídrico (HCl), por exemplo, possui um alto grau de ionização, pois cerca de 92% das suas moléculas são ionizadas em contato com a água. Já o ácido cianídrico (HCN), ao contrário, possui um baixo grau de ionização, pois cerca de apenas 4% de suas moléculas se ionizam.
Constante de Equilíbrio Iônico ou Constante de Ionização
Assim como no equilíbrio químico, o equilíbrio iônico também possui uma expressão que define as quantidades de produtos e reagentes no estado de equilíbrio, que é denominada constante de ionização.
Essa constante é representada por Ki, mas também pode ser chamada de Ka (constante de acidez) para os ácidos e Kb (constante de basicidade) para as bases. Podemos calcular ambas constantes através das fórmulas:
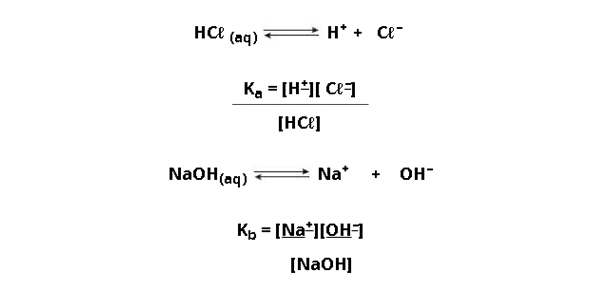
Valores da Constante de Ionização
- Quando o valor de Ki é alto, o valor de α é mais próximo de 100%, isso significa que a taxa de ionização é alta. Quando isso acontece, pode-se dizer que se trata de um ácido ou base forte;
- Quando o valor de Ki é baixo, o valor de α é mais próximo de 0%, isso significa que a taxa de ionização é baixa. Quando isso ocorre, pode-se dizer que se trata de um ácido ou base fraco.
Quando 100% das moléculas do ácido ou da base se ionizam, pode-se dizer que não se trata de um estado de equilíbrio iônico, uma vez que a reação possui apenas um sentido, não sendo uma reação reversível.
Além de aprender o que é Equilíbrio Iônico, você pode testar seus conhecimentos de outras matérias respondendo algumas questões que caíram em edições antigas do Exame em nosso simulado gratuito.
Gostou de aprender o que é Equilíbrio Iônico? Queremos te ajudar também a encontrar a FACULDADE IDEAL! Logo abaixo, faça uma pesquisa por curso e cidade que te mostraremos todas as faculdades que podem te atender. Informamos a nota de corte, valor de mensalidade, nota do MEC, avaliação dos alunos, modalidades de ensino e muito mais.
Experimente agora!





