As Funções Orgânicas são agrupamentos de substâncias químicas de acordo com o Grupo Funcional que elas possuem, uma parte da sua estrutura com características próprias. Essas funções podem ser os hidrocarbonetos, ésteres, álcoois, cetonas, aminas, ácidos carboxílicos e outros, sendo que cada uma possui sua utilidade no nosso cotidiano!
Neste artigo sobre o que são Funções Orgânicas, você encontrará todos os tópicos abaixo. Clique em um deles para ir diretamente ao assunto:
- Introdução à Química Orgânica: o átomo de carbono e as formas de representar cadeias
- Classificação das cadeias (elemento, ligação, formato e anel aromático).
- O que são Funções Orgânicas.
- Nomenclatura de compostos, regras para formação de nomes, ordem de numeração das cadeias e nomes das ramificações.
- Hidrocarbonetos.
- Funções oxigenadas: Álcool, Fenol, Aldeído, Cetona, Ácido carboxílico, Éter e Éter.
- Funções Nitrogenadas: Aminas, Amidas e Nitrocompostos.
- Haletos Orgânicos.
- Simulado online e gratuito de qualidade é só no Beduka! Você pode até personalizar com as matérias que preferir!
Introdução à Química Orgânica
A química orgânica é o ramo responsável por estudar os compostos orgânicos, cuja principal característica é ter a presença do átomo de carbono (C). Proteínas, carboidratos, lipídios, vitaminas e enzimas são exemplos de moléculas orgânicas.
Contudo, nem todo composto que possuir carbono será orgânico, exemplo disso é o gás carbônico (CO2).
Por isso, a definição mais completa é que uma molécula será orgânica se possuir carbono conjugado com alguns dos elementos: carbono (C), hidrogênio (H), oxigênio (O), nitrogênio (N), fósforo (P) e enxofre (S).
O átomo de Carbono (C)

Quando dizemos “conjugações”, referimos às ligas que se formam entre o átomo de carbono e os demais elementos.
Ao olhar a tabela periódica, sabemos que o C possui 4 elétrons (e-) de valência (na sua última camada atômica). Isso significa que estes 4 e- são os responsáveis por fazer 4 ligações covalentes e unir o carbono com outros elementos, formando cadeias.
Assim como o C precisa fazer 4 ligações para ficar estável, cada elemento possui seu número. O H só faz 1, o O costuma fazer 2 e assim por diante.
Como são os e- de valência que definem o número de ligações que o elemento pode fazer, você precisará consultar a tabela periódica e olhar a qual família (grupo) o elemento pertence. Se não tiver tabela, você deve saber de cór esses 3 elementos principais ou a questão te dará os dados.
As ligações podem ser simples (chamada de sigma), duplas (uma sigma e uma pi) ou triplas ( 2 sigmas e uma pi). Apesar de o Carbono poder fazer até 4 ligações, não existe ligação quádrupla, pois seria instável demais.
Formas de representação das cadeias carbônicas
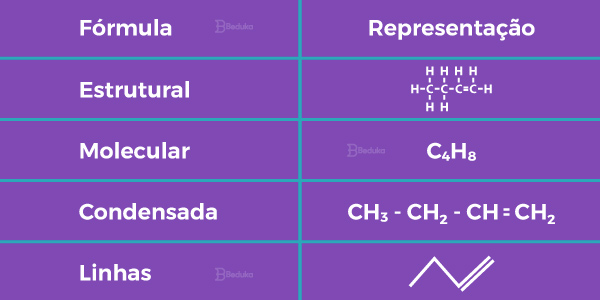
Como as cadeias podem se tornar longas, surgiram diferentes formas de representá-las. Cada uma delas tem sua vantagem ou desvantagem, mas você deve conseguir fazer uma boa leitura das principais formas:
- Fórmula molecular: a mais conhecida, em que se escreve por extenso os elementos que compõe e a quantidade deles, mas não há representação de ligações.
- Fórmula estrutural (com representação dos elétrons ou não): todas as estruturas ficam e elementos ficam evidentes, mas dá mais trabalho de fazer.
- Fórmula em linhas ou bastão: boa para escrever compostos grandes, longas cadeias, mas os átomos de hidrogênio ficam implícitos e cada quina corresponde a um carbono. Os heteroátomos são representados.
- Fórmula condensada: é um tipo mais prático de fórmula estrutural em que se une carbonos e hidrogênios
Classificação das cadeias carbônicas

As ligações formam cadeias de elementos conectados, e cada cadeia possui uma classificação. Elas variam conforme o tipo de ligação, dos elementos que a compõe e seu formato.
Quanto aos elementos
- Cadeias carbônicas homogêneas: apresentam apenas átomos de carbono e hidrogênio.
- Cadeias carbônicas heterogêneas: as que apresentam heteroátomo (algum dos demais elementos orgânicos que esteja entre carbonos: O,N,P,S).
Quanto aos tipos de ligação
- Cadeias carbônicas saturadas: apresentam apenas ligações simples entre carbonos.
- Cadeias carbônicas insaturadas: apresentam alguma ligação dupla ou tripla entre carbonos.
Quanto ao formato da cadeia
- Cadeias carbônicas abertas: também chamadas de acíclicas ou alifáticas, possui no mínimo 2 extremidades.
- Cadeias carbônicas fechadas: também chamadas de cíclicas, não possui extremidades.
- Cadeias carbônicas mistas: possuem um ciclo e ao menos uma extremidade ao mesmo tempo.
As cadeias abertas podem ser de dois tipos:
- Cadeias carbônicas lineares: Também chamada de reta ou normal, quando possui apenas 2 extremidades.
- Cadeias carbônicas ramificadas: Quando possui 3 ou mais extremidades.
Quanto à presença de um anel aromático
- Cadeias Carbônicas Aromáticas: em que há presença de um anel aromático.
- Cadeias Carbônicas Alicíclicas ou não-aromáticas: não há um anel aromático.
Existe uma estrutura específica que recebe o nome de Anel aromático. Ele é um tipo especial (e bem importante) de ciclo, em que há sempre 6 carbonos com ligações alternadas em duplas e simples.
Essas ligações estão sempre se movimentando lá dentro, por isso, o anel pode ser representado com uma circunferência desenhada em seu interior. Esse fenômeno se chama ressonância de elétrons e confere algumas capacidades especiais.
O que são Funções Orgânicas?
Os compostos orgânicos possuem diferentes utilidades, por isso separamos eles em funções orgânicas para facilitar a busca por algum específico.
Cada função possui um Grupo Funcional que a identifica, ou seja, uma característica na estrutura que é responsável por dizer se a substância X entra ou não naquela classificação.
São as 12 principais funções orgânicas:
Hidrocarboneto, Álcool, Fenol, Aldeído, Cetona, Ácido Carboxílico, Éster, Éter, Amina, Amida, Nitrocomposto e Haleto Orgânico!
Nomenclatura de compostos orgânicos
Antes de continuar, precisamos saber de alguns últimos conceitos: você já observou que as operações matemáticas e o sistema numéricos são internacionais?
Os cálculos e números que aprendemos no Brasil são os mesmos nos EUA ou na Europa. Apesar de culturas e idiomas diferentes, qualquer alfabetizado de qualquer nação ocidental é capaz de entender que 2+2=4 !
Por isso a IUPAC (União Internacional de Química Pura e Aplicada, em português), foi criada. Ela é uma organização que padroniza as questões químicas para que qualquer cientista de qualquer país “fale a mesma língua”!
Assim, foram estabelecidas algumas regras para dar nome aos compostos de acordo com sua estrutura. Qualquer entendido que bater o olho naquele nome, saberá qual é o composto em questão, seja um britânico ou um argentino!
Regras de nomenclatura dos compostos orgânicos
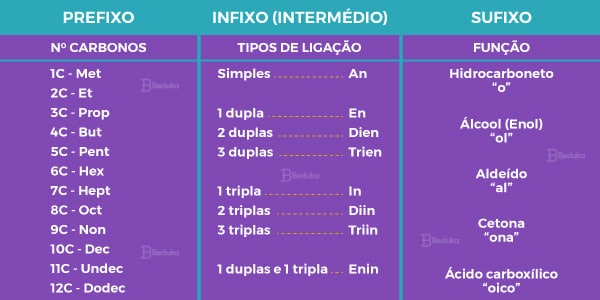
De modo geral, os nomes são sempre formados por três partes e cada uma expressa informações valiosas:
- Prefixo: indica o número dos átomos de carbono que aquele composto tem.
- Intermédio: indica o tipo de ligação que existe entre os átomos de carbono.
- Sufixo: indica qual é a função orgânica a qual o composto pertence.
Exemplo
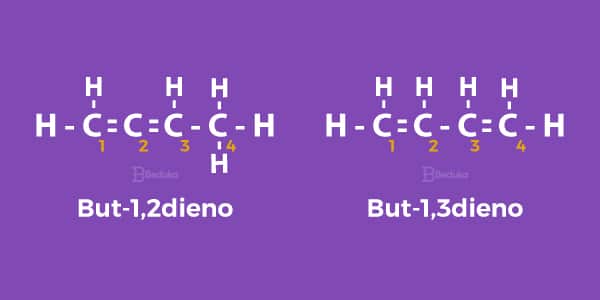
1) Vamos analisar os nomes But-1,2dieno e But-1,3dieno
- Prefixo BUT: 4 carbonos
- Intermediário DIEN: duas ligações duplas
- Sufixo O: função hidrocarboneto
O número 1 e 2 do primeiro nome indicam que as ligações duplas estão localizadas respectivamente no primeiro e no segundo carbono da cadeia.
Já no segundo composto, as ligações duplas estão no primeiro carbono e no terceiro.
Não devemos focar nas ligações, e sim nos carbonos. Depois, olhamos para as 4 ligações que os carbonos têm em volta.
Fazendo esse exercício você verá que não existe “but-1,4-dieno”, pois a ligação dupla pertence ao C que vier primeiro na ordem de contagem.
Ordem de numeração das cadeias
Para saber a ordem de numeração dos carbonos da cadeia, deve-se levar em conta algumas regras. Quando essas regras entrarem em conflito, prevalece a seguinte importância:
1°grupo funcional / 2°ligações / 3° ramificações
- Se houver um grupo funcional, a numeração deve começar do carbono que estiver mais próximo do grupo funcional.
- Se possuir uma ligação dupla, a contagem do primeiro carbono deverá ser um daqueles que compõe a ligação dupla. Como consequência, o segundo carbono da cadeia será o outro carbono que compõe da ligação dupla. Se houver um grupo funcional, essa regra perde força e o contagem começa do C próximo ao grupo funcional. Contudo, as ligações duplas e triplas deverão estar na cadeia principal!
- Se for uma cadeia ramificada, pegamos uma extremidade qualquer para contar e testamos todas as possibilidades, até encontrar uma sequência em que haja o maior número de carbonos na cadeia principal (a parte que não é ramificação).
Nomes das ramificações
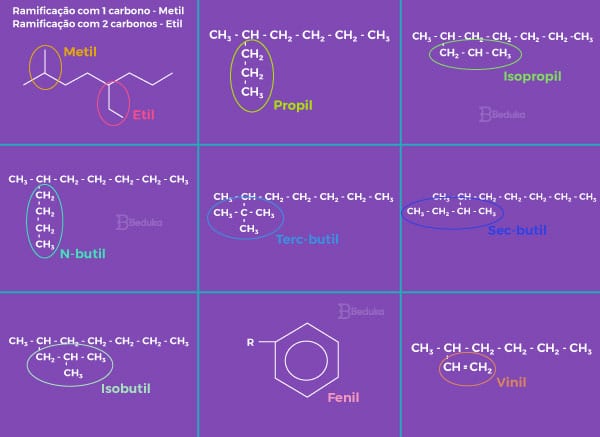
Separado o que é cadeia principal e o que é ramificação, a enumeração começa do carbono mais próximo à ramificação, se não houver ligações duplas ou grupos funcionais. Se houver, segue a ordem de importância das regras.
No nome do composto, escrevermos as ramificações e seus números de posição primeiro, depois o restante do nome normalmente.
Os formatos de ramificação possuem nomes próprios e se houver mais de uma no composto, elas serão escritas em ordem alfabética, desconsiderando os prefixos dos nomes da ramificação (di, tri…)
Veja a imagem abaixo com o nome dos radicais (ramificações) e lembre-se que “R” indica que alí há uma cadeia carbônica (hidrocarboneto).
Hidrocarboneto

- Característica: Possui apenas átomos de carbono e hidrogênio (C e H)
- Nomenclatura: Prefixo + intermédio + sufixo “o”
- Exemplos: Metano, butano, eteno… e um outro bem famoso: petróleo!
Observação:
Os nomes “alcanos” , “alcenos”, “alcadienos”, são utilizados para denominar qualquer hidrocarboneto com o referido tipo de ligação, assim como vimos nas regras de nomenclatura. São nomes genéricos.
- São mais de 200 resumo diários no Instagram do Beduka!
Funções orgânicas Oxigenadas
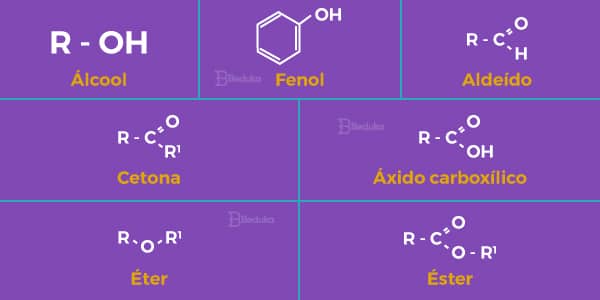
As funções orgânicas seguintes são aquelas caracterizadas pela presença de Oxigênio no Grupo Funcional (O).
Na imagem acima, há o desenho de todos os Grupos Funcionais de cada função oxigenada. Leia as características de cada uma e volte aqui para conferir a imagem e facilitar sua compreensão!
Lembre-se que “R” é a letra utilizada para indicar que alí há uma cadeia carbônica (hidrocarboneto)
Função Álcool
- Grupo Funcional: Possui a hidroxila (-OH) ligada a um carbono saturado
- Nomenclatura: Prefixo + intermédio + sufixo “ol”
- Exemplos: Metanol, propanol…e alguns outros bem famosos: álcool gel e cachaça possuem o etanol como principal constituinte
Os Álcoois que apresentam uma única hidroxila são classificados como monoálcoois, os que possuem duas hidroxilas são classificados como diálcoois, os que possuem três são triálcoois e os que possuírem 4 ou mais hidroxilas são classificados como poliálcoois.
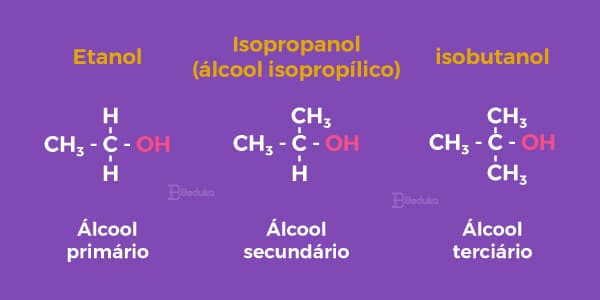
Os monoálcoois podem ainda ser classificados em:
Primários: quando a hidroxila está ligada a um carbono primário (C ligado a apenas 1 C).
Secundários: quando a hidroxila está ligada a um carbono secundário (C ligado a 2 C).
Terciários: quando a hidroxila está ligada a um carbono terciário (C ligado a 3 C).
Função Fenol
- Grupo Funcional: Possui a hidroxila (-OH) ligada a um carbono do benzeno (anel aromático), substituindo um H.
- Nomenclatura: localização do grupo OH + hidróxi + nome do aromático
- Exemplos: 1-hidroxi-2-metil-benzeno
Função Aldeído
- Grupo Funcional: Possui a carbonila (C=O) ligada a um hidrogênio (-CHO), sempre numa extremidade da cadeia
- Nomenclatura: Prefixo + intermédio + sufixo “al”
- Exemplos: Metanal (em solução aquosa é o formol)
Função Cetona
- Grupo Funcional: Possui a carbonila entre dois carbonos
- Nomenclatura: Prefixo + intermédio + sufixo “ona”
- Exemplo: Propanona (a “acetona” usada para tirar esmalte)
Função Ácido Carboxílico
- Grupo Funcional: Possui a carbonila ligada ao C que contém uma hidroxila (-COOH)
- Nomenclatura: Ácido + prefixo + intermédio + sufixo “oico”.
- Exemplos: Ácido metanóico (conhecido como ácido fórmico, gera ardência na picada da “formiga lava-pé”) e ácido etanóico (conhecido como ácido acético, é o que forma o vinagre).
Como o próprio nome aponta, uma das características desses compostos é ter o PH muito ácido!
Função Éster
- Grupo Funcional: É como um derivado dos ácidos carboxílicos, pois houve a substituição do hidrogênio da hidroxila por outra cadeia orgânica
- Nomenclatura: Prefixo + intermédio + sufixo “oato“ / de / nome do radical + ila
- Exemplos: Os aromas sintéticos utilizados em guloseimas são ésteres: Etanoato de pentila (aroma de banana), butanoato de etila (aroma de morango) e etanoato de isopentila (aroma de pêra).
Função Éter
- Grupo Funcional: Possui o oxigênio entre dois carbonos: (C ─ O ─ C)
- Nomenclatura: prefixo da menor cadeia + sufixo “oxi” + hidrocarboneto maior
- Exemplos: met-oxi-etano (metoxietano), et-oxi-etano (etoxietano)
Funções orgânicas Nitrogenadas

As funções orgânicas seguintes são aquelas caracterizadas pela presença de Nitrogênio no Grupo Funcional (N).
Na imagem abaixo há o desenho de todos os Grupos Funcionais de cada função nitrogenada, leia as características de cada uma e volte aqui para conferir a imagem e facilitar sua compreensão!
Lembre-se que “R” é a letra utilizada para indicar que alí há uma cadeia carbônica (hidrocarboneto).
Função Amina
- Grupo Funcional: Deriva da substituição de um ou mais hidrogênios da amônia (NH3) por cadeias carbônicas
- Nomenclatura: Prefixo + intermédio + sufixo “amina”
- Exemplos: Metilamina, etilamina, trimetilamina (substâncias responsáveis pelo cheiro rançoso de peixe)
Como são derivadas das amônias, uma das características desses compostos é ter o PH básico!
Função Amida
- Grupo Funcional: Também utilizamos o raciocínio da derivação da amônia pela substituição de um de seus hidrogênios por um grupo acila, um carbono insaturado (C=O)
- Nomenclatura: Prefixo + intermédio + sufixo “amida”.
- Exemplos: metanamida e etanamida.
Função Nitrocomposto
- Grupo Funcional: Possui o grupo nitro (NO2) ligado a uma cadeia carbônica
- Nomenclatura: nitro + prefixo + intermédio + sufixo “o”
- Exemplos: nitrometano, nitroetano e 2-metil-1,3,5-trinitrobenzeno (TNT, o explosivo)
Compostos Halogenados: Função Haleto Orgânico
- Grupo Funcional: Possui um ou mais halogênios (F, Cl, Br ou I) ligados a uma cadeia carbônica
- Nomenclatura: quantidade de halogênios + nome do halogênio + nome do hidrocarboneto
- Exemplos: 2-bromopropano, clorobenzeno e 1,3-difluorobutano.
Gostou do nosso artigo sobre o que são Funções Orgânicas? Confira outros artigos do nosso blog e se prepare para o Enem da melhor maneira! Você também pode se organizar com o nosso plano de estudos, o mais completo da internet, e o melhor: totalmente gratuito!
Queremos te ajudar a encontrar a FACULDADE IDEAL! Logo abaixo, faça uma pesquisa por curso e cidade que te mostraremos todas as faculdades que podem te atender. Informamos a nota de corte, valor de mensalidade, nota do MEC, avaliação dos alunos, modalidades de ensino e muito mais.
Experimente agora!






8 Comentários
A representação das amidas é essa mesmo?
Sim Mauro.
O conteúdo do texto está correto. Pode confiar.
A imagem da amida está correta mas está escrito errado. Está escrito amina onde deveria estar escrito amida, na 11ª imagem, no tópico Funções orgânicas Nitrogenadas.
Bem notado, Diogo! Já foi atualizado.
Não entendo nada de Química, e a partir de agora irei estuda pelo conteúdo de vocês. Espero poder contar com o BEDUCA.
Obrigada pelo Blog.
Ei, Idalina. Conte conosco e logo logo você estará fera na Química!
espero que eu consiga me sair bem no enem
Com os nossos conteúdos você vai conseguir!