A cinética química é a área que estuda a velocidade das reações, bem como os fatores que influenciam essa velocidade. A rapidez de uma reação química indica a variação da quantidade de reagentes e produtos com o passar do tempo.
Se você vai prestar vestibular tem que saber o que é cinética química. Se você ainda não sabe do que se trata a gente te explica com um conteúdo completo que pode fazer com que você gabarite as questões desse tema. Você também pode testar seus conhecimentos de química e de outras matérias no nosso simulado.
Escrevemos um resumo de química com as matérias que mais caem no enem, também temos artigos sobre química orgânica e química inorgânica para você aprender facilmente.
Se você está preocupado com a prova de Ciências da Natureza e suas tecnologias, fique calmo. Além dos conteúdos de química, o Beduka te ajuda a estudar para a prova com nossos conteúdos de física e biologia. Saiba aqui qual a definição de movimento uniforme, qual a função do núcleo da célula ou até mesmo faça algumas questões sobre genética, que é um tema recorrente na prova.
Neste artigo vamos te explicar o que é cinética química, dar exemplos e dicas para que você entenda melhor sobre o assunto e se dê bem na prova.
Estude com o simulado do Beduka. É grátis!
O que é cinética química?
Cinética química é a matéria que estuda a velocidade das reações químicas e os fatores que influenciam essas reações.
Faça também os Exercícios de Cinética!
Podemos definir reações químicas como o resultado de ações entre duas ou mais substâncias que dão origem a diferentes compostos. Equação química é a representação gráfica de uma reação química, onde os reagentes aparecem no primeiro membro e os produtos, no segundo.

Velocidade das reações químicas
O que determina a velocidade de uma reação química é o tempo em que os reagentes são consumidos para formar produtos. A velocidade de uma reação pode ser representada tanto pelo consumo de um reagente, quanto pela geração de um produto.
Antes de ocorrer a reação química temos uma quantidade máxima de reagentes e nenhum produto. Quando um dos reagentes é totalmente consumido, os produtos se formam e a reação termina.
Classificação das reações químicas
Para entender melhor a cinética química é preciso saber que as reações químicas podem ser classificadas de 3 maneiras:
- Reações rápidas: São aquelas que ocorrem instantaneamente, em questão de microssegundos. Um exemplo é a queima do gás de cozinha.
- Reações moderadas: São aquelas que levam de minutos a horas para serem finalizadas. Um exemplo é a queima do papel.
- Reações Lentas: São aquelas que podem durar séculos, pois os reagentes combinam-se lentamente. Um exemplo é a formação do petróleo.
Teoria das colisões
A teoria das colisões é aplicada para reações gasosas. Ela determina que para a reação química aconteça os reagentes devem estar em contato, através de colisões.
Apenas isso não garante que a reação ocorra. É necessário também que as colisões sejam efetivas, pois isso irá garantir que as moléculas adquiram energia suficiente, a energia de ativação.
A energia de ativação é a energia mínima necessária para que ocorra a efetiva realização da reação.
O complexo ativado é um estado transitório da reação, entre os reagentes, enquanto os produtos finais ainda não foram formados.
Fatores que influenciam na velocidade da reação química
Alguns fatores podem alterar a velocidade de uma reação química. São eles:
- Natureza dos reagentes
- Temperatura
- Pressão
- Superfície de contato
- Presença de agentes externos
A seguir vamos explicar como cada um desses fatores tem influência na velocidade da reação.
Natureza dos reagentes
A velocidade da reação química depende de características intrínsecas de seus reagentes. Dessa forma, há uma ampla faixa de velocidades.
Temperatura
Temperatura é uma medida de energia cinética, que corresponde ao grau de agitação das partículas. Quando a temperatura é alta, as moléculas estão mais agitadas, aumentando a velocidade da reação. Quanto maior é a temperatura, maior a velocidade da reação química.
Há uma regra que foi formulada no século XIX pelo holandês Jacobus Henricus van’t Hoff que diz que se ocorrer um aumento de 10 graus celsius na temperatura da reação, ela irá reagir duplicando a velocidade da reação. Hoje sabe-se que essa regra apresenta várias exceções, mas ela é muitas vezes útil para fazerem previsões aproximadas do comportamento da velocidade de certas reações. Ela é conhecida como Regra de Van’t Hoff.
Pressão
Essa condição afeta apenas reações que tenham pelo menos uma substância gasosa como reagente. O aumento da pressão faz com que o espaço entre as moléculas diminua, dessa forma elas têm mais colisões e a velocidade da reação aumenta.
Superfície de contato
Em solução ou em fase gasosa, os reagentes são capazes de se misturarem completamente e de colidirem entre si facilmente (reação homogênea). Mas em reações heterogêneas os reagentes só fazem contato na interface. Neste caso, a velocidade das reações depende da área de contato entre as fases.
Presença de agentes externos
Agentes externos são algumas substâncias que afetam a velocidade das reações químicas sem serem consumidos na reação, permanecendo inalterados quando a reação termina.
- Catalisadores: aumentam a velocidade da reação.
- Inibidores: diminuem a velocidade da reação.
Como, normalmente, os químicos estão mais interessados em acelerar as reações químicas, os catalisadores são mais investigados. No entanto, existem várias reações que ocorrem na natureza e que são indesejáveis, como por exemplo a corrosão de metais. Este tipo de reação não pode ser impedida, mas inibidores podem retardá-las.
Velocidade média
É necessário entender a velocidade média de uma reação (Vm). Assim como na física, a velocidade da reação é calculada pela expressão:
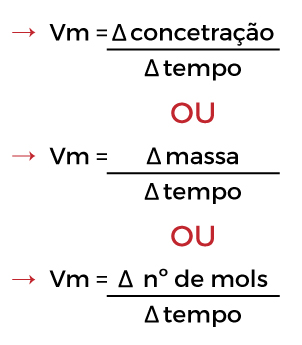
A velocidade de uma reação depende do número de choques entre as moléculas dos reagentes e da energia com que as moléculas colidem entre si.
Gostou de aprender o que é cinética química? Comente e compartilhe. Siga o Beduka no Facebook e no Instagram.
O Beduka te ajuda a passar no vestibular
Além de explicar o que é cinética química, já falamos aqui sobre outros assuntos que caem nos vestibulares. Aproveite para aprender de uma vez por todas a fazer cálculo estequiométrico e a entender o que é um átomo neutro. Você também pode fazer algumas questões sobre a origem da vida.
O Beduka é um buscador de universidades e cursos superiores reconhecidos pelo Ministério da Educação (MEC) que surgiu em 2017. Aqui em nosso site o estudante pode conferir diversas informações para encontrar a melhor faculdade para a graduação que deseja fazer. Experimente agora!
Agora que você aprendeu o que é cinética química, você também pode ver uma relação com as melhores relações para cada curso. Conheça as melhores faculdades de relações internacionais, de economia e de filosofia do Brasil.
Você acabou de conferir uma breve explicação de o que é cinética química, aproveite também para ler resumos de alguns dos livros que mais caem nos vestibulares:
- Resumo do livro O Bem Amado de Gomes Dias
- Resumo de Os Lusíadas de Camões
- Resumo do livro Senhora de José de Alencar
Gostou do nosso texto sobre o que é cinética química? Compartilhe com os seus amigos e comente abaixo sobre áreas que você deseja mais explicações.
Queremos te ajudar a encontrar a FACULDADE IDEAL! Logo abaixo, faça uma pesquisa por curso e cidade que te mostraremos todas as faculdades que podem te atender. Informamos a nota de corte, valor de mensalidade, nota do MEC, avaliação dos alunos, modalidades de ensino e muito mais.
Experimente agora!





