A organização da tabela periódica consiste na forma de sistematizar e apresentar informações sobre todos elementos químicos que existem. Essa organização é feita com base na ordem crescente do número atômico, na configuração eletrônica dos átomos dos elementos, e de acordo com propriedades químicas semelhantes. Leia este resumo completo para ficar a par do assunto!
Se você quiser ir diretamente para alguma parte do texto, clique em um dos tópicos abaixo:
- Qual é a origem da tabela periódica?
- Como é a organização da tabela periódica?
- O que são as famílias da tabela periódica?
- O que são os períodos da tabela periódica?
- Nós conectamos você à faculdade!
Estudando Química para o Enem? Depois de aprender como ler a tabela periódica, teste seus conhecimentos com o Simulado Beduka do Enem. Ele é totalmente gratuito e personalizável, acesse agora!
Qual é a origem da Tabela Periódica?
A Tabela Periódica mais completa foi elaborada pelo químico russo Dmitri Mendeleiev em 1869, e foi organizada em função da massa atômica dos elementos. Mendeleiev organizou os elementos de acordo com as propriedades semelhantes e deixou espaços vazios para os elementos que ele acreditava que ainda seriam descobertos.
A Tabela Periódica atual foi elaborada por Henry Moseley em 1913, que realizou experimentos com raios X e descobriu o número atômico (Z) dos elementos químicos, ou seja, a quantidade de prótons que há no núcleo dos átomos de cada elemento. Moseley provou que as propriedades dos elementos tinham relação com o número atômico, e não com a massa atômica, como dizia Mendeleiev.
William Ramsay descobriu os elementos neônio, argônio, criptônio e xenônio. Esses elementos juntamente com hélio e radônio incluíram a família dos gases nobres na Tabela Periódica. Glenn Seaborg descobriu os elementos transurânicos (do número 94 a 102) e em 1944 propôs a reconfiguração da Tabela Periódica.
A tabela periódica completou 150 anos em 2019 e foi criada uma resolução das Nações Unidas e da UNESCO para que esse seja o Ano Internacional da Tabela Periódica dos Elementos Químicos como forma de reconhecimento a uma das criações mais influentes e importantes da ciência.
- Você sabe qual é o primeiro elemento da tabela periódica? Descubra essa e outras curiosidades aqui!
Como é a organização da Tabela Periódica?
A Tabela Periódica atual é organizada em linhas horizontais em ordem crescente de número atômico. Sendo o primeiro elemento químico que aparece da esquerda para a direita na parte superior o hidrogênio, que possui o menor número atômico (1).
Após ele, observa-se o hélio, que possui número atômico igual a 2, depois o lítio, com número atômico igual a 3, seguido do berílio, Be, de número atômico igual a 4, e assim por diante.
A classificação crescente de números atômicos permite organizar os elementos em grupos que possuem propriedades semelhantes, e que revelam particularidades a respeito dos átomos dos elementos.
- Quer saber mais sobre o assunto? Temos um artigo completo sobre os elementos da tabela periódica!
Grupos ou famílias – Colunas
As colunas são chamadas de grupos ou famílias. Os elementos pertencentes a um mesmo grupo ou a uma mesma família da Tabela Periódica possuem propriedades físicas e químicas semelhantes. Os elementos químicos que estão em uma mesma coluna possuem a mesma quantidade de elétrons na camada de valência, isto é, na última camada eletrônica:
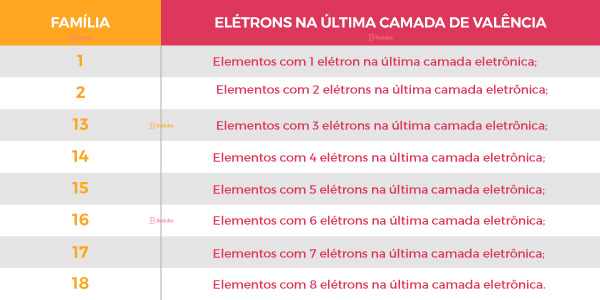
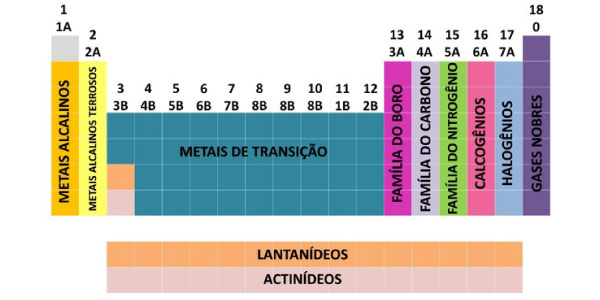
Segundo a IUPAC (União Internacional da Química Pura e Aplicada), as famílias da Tabela Periódica devem ser ordenadas de 1 a 18. Algumas dessas possuem nomes específicos:
- Família 1: Metais alcalinos;
- Família 2: Metais alcalino terrosos;
- Família 16: Calcogênios;
- Família 17: Halogênios;
- Família 18: Gases Nobres.
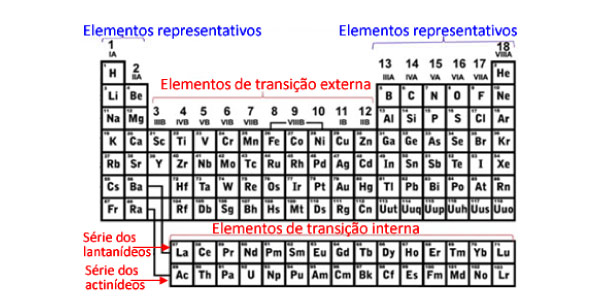
Elementos Representativos
Antigamente eram todos os membros das famílias que tinham o número acompanhado da letra “A” (1A, 2A, 3A, 4A, 5A, 6A, 7A e 8A). Atualmente, eles estão nas famílias 1, 2, 13 a 18 e possuem o seu elétron mais energético situado nos subníveis “s” ou “p”.
Elementos de Transição
Antigamente eram todos os membros das famílias que tinham o número acompanhado da letra “B” (1B, 2B, 3B, 4B, 5B, 6B, 7B e 8B). Atualmente, eles são os membros das famílias 3 a 12. Esses elementos estão representados na região central da Tabela e possuem o seu elétron mais energético situado nos subníveis “d” ou “f”.
- Elementos de transição externa: São os elementos que estão expostos regularmente como os demais elementos na Tabela Periódica. Eles estão representados na região central da Tabela. Seus elétrons mais energéticos ficam no subnível “d”.
- Elementos de transição interna: Esses elementos estão abaixo do corpo principal da Tabela e são divididos em duas séries: a série dos lantanídeos e a série dos actinídeos. Seus elétrons mais energéticos ficam no subnível “f”.
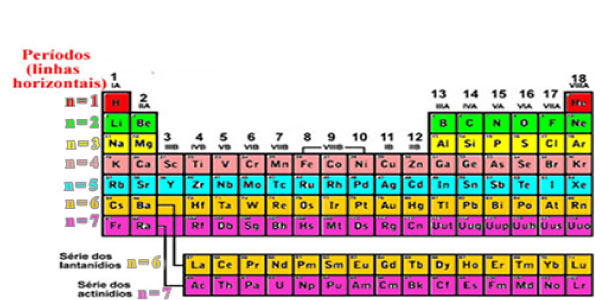
Períodos – Linhas
As sete linhas horizontais da Tabela Periódica são chamadas de períodos. Eles indicam a quantidade de camadas eletrônicas que os átomos que os elementos pertencentes a eles possuem.
Tomando como exemplo todos os elementos do primeiro período (primeira linha) da Tabela Periódica, observa-se que eles possuem apenas uma camada eletrônica, a camada K. Já os elementos do segundo período possuem duas camadas eletrônicas, as camadas K e L, e assim por diante.
- Agora que você já sabe como é a organização da tabela periódica, que tal testar o que aprendeu com os 18 melhores exercícios sobre o assunto?
Esperamos que este artigo sobre a organização da tabela periódica tenha despertado em você a vontade de estudar mais sobre o fantástico mundo da Química!
Logo abaixo temos uma oportunidade incrível para você, não deixe de conferir!
Nós conectamos você à faculdade!
Você sabia que é possível entrar na faculdade sem fazer o Enem? Sim! E o melhor, você pode realizar seu sonho e ainda economizar dinheiro.
Conheça o Beduka Bolsas, a plataforma do Beduka disponível 24 horas, onde você pode encontrar bolsas de estudo com até 65% da mensalidade!
Faça a faculdade dos seus sonhos, escolhendo entre mais de 90 opções de cursos em uma de nossas universidades parceiras.
Siga também o Beduka nas redes sociais! Em nosso Instagram você encontra todos os conteúdos que podem cair no Enem e no Pinterest os melhores resumos sobre todas as matérias cobradas no vestibular.
É tudo gratuito e pensado em te ajudar a entrar na faculdade!
Obrigada por ler nosso resumo sobre a organização da tabela periódica.





