A energia mínima necessária para que os elétrons sejam retirados de um átomo ou íon no estado gasoso é chamada de energia de ionização. Neste resumo, vamos abordar o que é energia de ionização, qual é sua função na ligação iônica e como você pode verificá-la na tabela periódica! Leia até o fim, pois esse tema certamente será útil para você no vestibular.
Se você quiser ir diretamente para alguma parte do texto, clique em um dos tópicos abaixo:
- O que é Ligação Iônica?
- O que é energia de ionização?
- Como identificar a energia de ionização na tabela periódica?
- Nós conectamos você à faculdade!
Estudando Química para o Enem? Depois de ler nosso resumo, teste seus conhecimentos com o Simulado Beduka do Enem. Ele é 100% gratuito e personalizável, acesse agora!
O que é Ligação Iônica?
Antes de definirmos o que é a energia de ionização, é interessante entender em que contexto ela aparece, ou seja, como acontece a ligação iônica.
A ligação iônica ocorre entre elementos eletropositivos (metais) e elementos eletronegativos (ametais e hidrogênio).
Nessa ligação, os metais apresentam a tendência em ceder seus elétrons, assim transformando-se em cátions (íons positivos). E os ametais e o hidrogênio, recebem esses elétrons e tornam-se ânions (íons negativos).
E o produto dessa ligação é chamado de composto iônico.
Em resumo: para que ambos os elementos presentes na ligação iônica tornem-se estáveis, ou seja, tenham oito elétrons na última camada, eles estabelecem essa relação de equilíbrio.
- Ainda está com dúvida? Leia nosso resumo completo sobre Ligação Iônica
Agora que você retomou seu entendimento sobre ligação iônica, vamos partir para o que interessa: compreender o que é energia de ionização e seu papel na ligação entre os átomos.
O que é energia de ionização?
A energia de ionização, também chamada de potencial de ionização, é uma propriedade periódica que pode ser definida como a energia mínima necessária para retirar elétrons de um átomo ou íon no estado gasoso.
Em outras palavras, podemos dizer que um átomo ou íon só perderá elétrons se receber energia suficiente.
A primeira energia de ionização, isto é, a remoção do primeiro elétron costuma ser a mais importante. Isso porque, sua energia de ionização é menor, pois seu elétron é o mais afastado do núcleo.
Como a força de atração com o núcleo é menor, é preciso menos energia e dessa forma é mais fácil removê-la.
Outra consequência decorrente da perda elétrons pelos átomos, é a diminuição do raio atômico.
Além disso, no caso dos íons, eles tornam-se cada vez mais positivos, portanto, a atração com o núcleo fica mais forte, necessitando mais energia para a retirada do próximo elétron e assim sucessivamente.
- O potencial de ionização é apenas uma das propriedades periódicas, veja aqui outras quatro e aprenda como ler a tabela periódica!
Depois de entender o que é energia de ionização, que tal aprender como identificá-la na tabela periódica? Confira a seguir!
Como identificar a energia de ionização na tabela periódica?
As propriedades periódicas dos elementos químicos são determinadas características que variam em intervalos regulares, de acordo com o aumento ou a diminuição dos números atômicos. E como mencionamos, a energia de ionização é uma propriedade periódica.
Na tabela periódica ela pode ser observada aumentando de baixo para cima e da esquerda para direita, portanto, sendo contrária ao raio atômico. Observe na tabela abaixo:
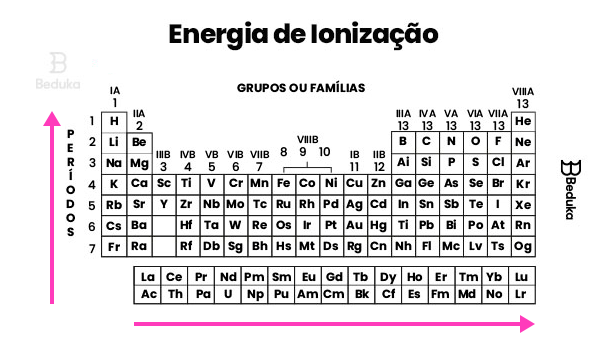
Esperamos ter contribuído com seus estudos com este resumo sobre o que é energia de ionização.
- Quer aprender mais sobre as ligações químicas e suas características? Leia nosso resumo completo sobre o assunto!
Seu sonho é entrar na faculdade? Não deixe de conferir a oportunidade perfeita que temos para você a seguir!
Nós conectamos você à faculdade!
Você sabia que é possível entrar em uma excelente universidade, no curso dos seus sonhos, sem fazer o Enem ou vestibular?
É isso mesmo! Estamos falando do Beduka Bolsas.
O Beduka Bolsas é uma plataforma online que te conecta com bolsas de estudos nas melhores universidades!
São mais de 90 opções de cursos para você escolher, com bolsas que podem chegar até 65% de desconto no valor da mensalidade, e de quebra, você ainda ganha a matrícula gratuita!
Você não pode perder essa oportunidade.
Siga o Beduka no Pinterest e Instagram e receba conteúdos diários e gratuitos sobre o mundo do Enem e Vestibulares.
Obrigada por ler até o final!






2 Comentários
Esta imagem da energia de ionização nos elementos da tabela periódica está errada.
Kenia, muito obrigado pelo aviso. Fizemos a substituição.