Você sabia que a maioria dos compostos existentes no universo são formados por ligações covalentes? Sim! Neste tipo de ligação química, ocorre o compartilhamento de elétrons da camada de valência entre átomos com alta eletronegatividade. Entenda o que é ligação covalente com nosso resumo completo sobre o assunto!
Neste resumo sobre o que é ligação covalente, você encontrará os tópicos abaixo. Se quiser, clique em um deles para ir diretamente ao conteúdo:
- O que é Ligação Covalente?
- Quais são os tipos de ligação covalente?
- Ligação covalente simples
- Ligação covalente dupla
- Ligação covalente tripla
- Ligação covalente dativa
- O que é a fórmula eletrônica de Lewis?
- Nós conectamos você à faculdade!
Estudando Química para o Enem? Pratique com as questões do Simulado Enem do Beduka! Ele é totalmente gratuito e personalizável.
O que é Ligação Covalente?
De acordo com a regra do octeto, para que os átomos tornem-se estáveis, eles precisam de 8 elétrons, ou 2 no caso do hidrogênio, em sua última camada (camada de valência).
Como sabemos, os únicos elementos estáveis naturalmente são os gases nobres. Portanto, todos os demais elementos precisam realizar ligações químicas, onde os átomos perdem, ganham ou compartilham seus elétrons.
Na ligação covalente há o compartilhamento de elétrons para a formação de moléculas estáveis. Essa interação acontece com átomos que apresentam alta eletronegatividade, ou seja, átomos que apresentam a capacidade de receber elétrons.
- A eletronegatividade é um tipo de propriedade periódica, descubra tudo sobre elas aqui!
Dessa forma, a ligação covalente pode ser encontrada em moléculas que envolvem ligações entre semimetais, ametais e hidrogênio.
O compartilhamento acontece quando um elétron da última camada passa a fazer parte da mesma nuvem eletrônica que envolve outro elétron da camada de valência de outro átomo.
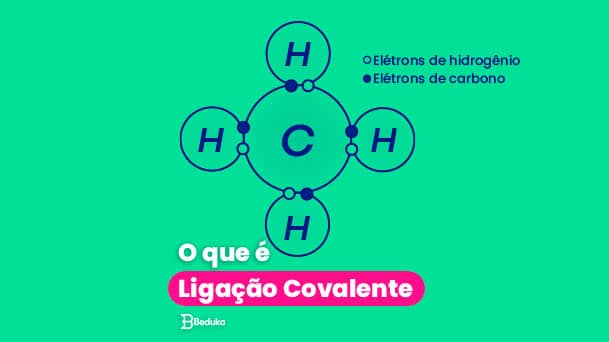
Para facilitar seu entendimento sobre o que é ligação covalente vamos utilizar o caso do gás hidrogênio (H2):
Cada átomo de hidrogênio apresenta apenas um elétron em sua camada de valência, assim, para garantir sua estabilidade, ele se junta a outro hidrogênio
Desse modo, os dois elétrons, um de cada átomo passam a fazer parte da mesma nuvem, e com a última camada completa, (que no caso do hidrogênio comporta apenas dois elétrons) ambos garantem a estabilidade.
Abaixo, listamos as principais características das moléculas unidas por ligação covalente:
- Pontos de Fusão e Ebulição baixos;
- Sólidos, líquidos ou gasosos em temperatura ambiente;
- Pouco solúveis;
- São mais inflamáveis;
- Não são bons condutores em meio aquoso.
Depois de compreender o que é a ligação covalente, descubra quais são seus diferentes tipos a partir de exemplos do cotidiano!
Quais são os 4 tipos de Ligação Covalente?
Há quatro diferentes formas dos átomos dos elementos semimetais, ametais e o hidrogênio ligarem-se a outros átomos a partir do compartilhamento de seus elétrons.
Tudo depende de quantos elétrons cada elemento precisa para completar a regra do octeto. E podemos descobrir isso de forma bastante simples, basta olhar a qual família pertence o elemento.
O número de cada família indicará quantos elétrons o átomo de determinado elemento possui na camada de valência, e sabendo disso, podemos determinar quantos elétrons ele precisará compartilhar para ficar estável.
A seguir, te mostramos os diferentes tipos de ligações com exemplos, para você entender o que é ligação covalente de forma completa.
Ligação covalente simples
Ok, talvez este exemplo sobre o que é ligação covalente simples não esteja presente em seu cotidiano, mas ele foi extremamente importante no contexto da Primeira Guerra Mundial!
Estamos falando do gás cloro (Cl2), que foi utilizado como arma química, devido sua alta toxicidade. Ele provoca irritações na garganta e lacrimejamento e em concentrações mais elevadas causa danos ao pulmão e pode levar à morte.
Na ligação covalente simples, o átomo compartilha somente um elétron de sua última camada com outro átomo e vice-versa. No gás cloro, os átomos de cloro “dividem” seu elétron da última camada entre si.
Ligação covalente dupla
Neste tipo de ligação, os átomos compartilham dois elétrons da camada de valência entre si.
O dióxido de carbono (CO2), também conhecido como gás carbônico, é um exemplo de ligação covalente dupla, pois cada oxigênio compartilha dois elétrons com o átomo de carbono.
O gás carbônico é um composto químico que apresenta um importante papel na manutenção da vida no planeta Terra.
No ciclo biogeoquímico do carbono, o gás é liberado para a atmosfera através da respiração, materiais residuais, combustão e decomposição de organismos e é absorvido pelas plantas no processo de fotossíntese.
Entretanto, depois da Revolução Industrial, com a queima de combustíveis fósseis e demais atividades humanas, a concentração de CO2 na atmosfera aumentou drasticamente, intensificando o efeito estufa.
- Depois de ler nosso resumo completo sobre o que é ligação covalente, coloque seus conhecimentos em prática com os 8 melhores exercícios sobre ligações químicas!
Ligação covalente tripla
Nessa ligação os átomos “dividem” três elétrons de cada elemento em busca da estabilidade.
Podemos citar o gás nitrogênio como exemplo sobre o que é ligação covalente tripla, em que cada átomo de nitrogênio compartilha três elétrons entre si.
O gás nitrogênio é considerado o mais abundante no ar atmosférico, compondo aproximadamente 78% de seu volume em massa.
Além disso, por ser pouco reativo e não inflamável, ele costuma ser empregado no preenchimento de bulbos de lâmpadas, no empacotamento de alimentos e no enchimento de pneus.
Ligação covalente dativa
Diferente das ligações que citamos anteriormente, além do compartilhamento de elétrons, nessa ligação também ocorre a transferência dos pares eletrônicos disponíveis.
Esse tipo de ligação acontece com os átomos do dióxido de enxofre (SO2).
Quando se dá a formação deste gás, ocorre o compartilhamento de dois elétrons de oxigênio com um átomo de enxofre e a doação de um par de elétrons do oxigênio para outro átomo de enxofre.
O SO2 é emitido de forma natural através de atividades vulcânicas e também por atividades humanas industriais e meios de transporte. Ele é amplamente utilizado como gás de refrigeração e na preservação de frutas secas, refrigerantes e vinhos.
O que é a Fórmula Eletrônica de Lewis?
E para finalizar nosso resumo sobre o que é ligação covalente, você vai conhecer uma forma bastante didática de demonstrar como essas ligações acontecem.
Em 1916, o químico norte-americano Gilbert N. Lewis, que também foi responsável pelo desenvolvimento da regra do octeto, propôs uma maneira de representar as ligações covalentes.
Essa fórmula é importante, pois além de mostrar os elementos e o número de átomos envolvidos, ela também representa os elétrons da última camada de cada átomo e quantos são os pares eletrônicos compartilhados por cada átomo.
Chamamos ela de fórmula eletrônica de Lewis: onde os elétrons da camada de valência são representados por bolinhas ou x e são dispostos em volta do símbolo do elemento químico.
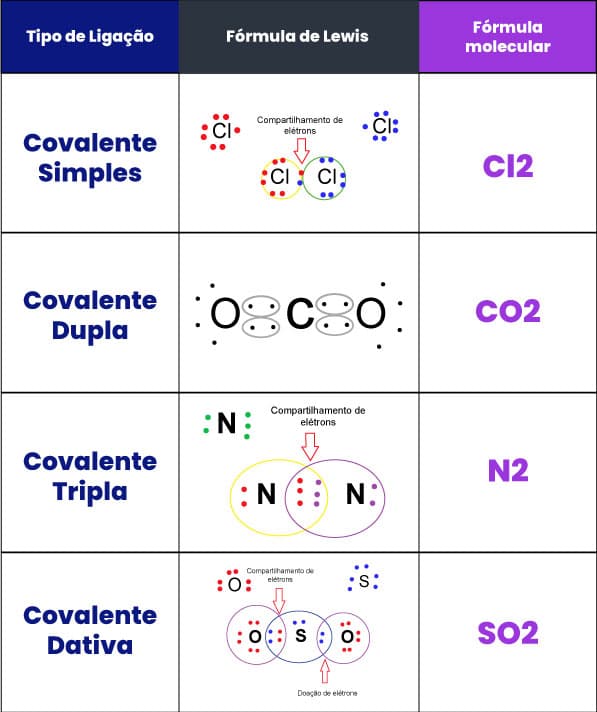
Os elétrons compartilhados são colocados lado a lado, como nos exemplos da tabela:
Esperamos ter respondido sua dúvida sobre o que é ligação covalente com este resumo.
O Beduka é o seu maior parceiro quando o assunto é entrar na faculdade. A seguir temos uma oportunidade incrível para você!
Nós conectamos você à faculdade!
Você sabia que é possível entrar na faculdade sem fazer o Enem? Sim! E o melhor, você pode realizar seu sonho e ainda economizar dinheiro.
Conheça o Beduka Bolsas, o programa do Beduka onde você pode encontrar bolsas de estudo com até 65% da mensalidade!
Faça a faculdade dos seus sonhos, escolhendo entre mais de 90 opções de cursos em nossas universidades parceiras. Temos Direito, Enfermagem, Psicologia e muito mais!
Siga também o Beduka nas redes sociais! Em nosso Instagram você encontra todos os conteúdos que podem cair no Enem e no Pinterest os melhores resumos sobre todas as matérias cobradas no vestibular. É tudo gratuito e pensado em te ajudar a entrar na faculdade!
Obrigada por ler até o final.