A separação de misturas é o processo de afastar substâncias diferentes que antes estavam juntas em uma mistura. As misturas podem ser heterogêneas ou homogêneas e isso influencia na escolha de um método para realizar a separação eficaz.
Neste artigo sobre separação de misturas, você encontrará:
- O que são misturas homogêneas e heterogêneas
- Importância da separação de misturas
- Métodos de separação de misturas homogêneas e heterogêneas
- Exemplos
- Estudando para as provas? Conheça O melhor Simulado do Brasil! Ele pode ser personalizado com as matérias que você mais precisa!
O que são misturas?
Na química, “mistura” é definida como a combinação de duas ou mais substâncias. Dependendo do modo como essas substância irão se relacionar, as misturas podem ser classificadas em homogêneas ou heterogêneas.
Vamos entender a diferença entre elas:
Misturas homogêneas ou soluções
As misturas homogêneas, também chamadas de soluções, são aquelas que possuem fase única. Isso significa que, quando olhamos a olho nu, vemos uma mistura perfeita. Dessa forma, só conseguimos identificar um aspecto uniforme.
Exemplo:
Ao misturar água e álcool, eles se misturam de forma que não conseguimos enxergar separadamente o que é álcool e o que é água. Eles se tornam um, então dizemos que são miscíveis!
Misturas heterogêneas
As misturas heterogêneas são aquelas que possuem duas ou mais fases. Isso significa que, quando olhamos a olho nu, vemos uma divisória entre os componentes. Dessa forma, não há um aspecto uniforme.
Exemplo:
Ao misturar água e óleo, eles formam uma mistura com duas fases: vemos o óleo em cima e a água abaixo. Isso significa que eles não são miscíveis.
Atenção!
Você já deve ter ouvido falar que “água e óleo não se misturam” e por isso pode ter achado estranho nós termos dito que eles formam uma mistura.
A questão é que o vocabulário popular nem sempre está de acordo com o científico…
Na realidade, qualquer recipiente que contenha duas ou mais substâncias são sim uma mistura. Então, água e óleo se misturam embora não sejam miscíveis, ou seja, eles não formam uma mistura homogênea, mas formam uma heterogênea.
Para facilitar o entendimento, veja mais alguns exemplos:
- água + sal ⟶ mistura homogênea ou monofásica
- soro caseiro (água + açúcar + sal) ⟶ mistura homogênea ou monofásica
- areia + óleo ⟶ mistura heterogênea bifásica
- água + acetona + terra ⟶ mistura heterogênea bifásica (água e acetona são miscíveis, contam como 1 fase apenas)
- chocolate + passas + castanhas ⟶ mistura heterogênea trifásica
Qual é a importância dos métodos de separação de misturas?
Separação de misturas é o nome que se dá a qualquer processo utilizado para separar duas ou mais substâncias.
A separação de misturas é muito importante e está mais presente no nosso dia a dia do que imaginamos.
A maioria dos materiais encontrados na natureza são misturas, então precisamos saber os métodos de separação para termos acesso ao que queremos extrair. Só depois disso teremos a matéria-prima adequada para fazer novas combinações e produzir novas coisas.
Veja alguns exemplos:
- Separação da água do mar para obter sal;
- Tratamento da água;
- Coleta e reciclagem de lixo;
- Produção de metais;
- Produção de medicamentos, alimentos, bebidas, higiene e limpeza;
- Análise do sangue em laboratório.
Observação: normalmente a separação dos componentes de uma mistura quase sempre é feita com mais de um método!
Quais são os métodos de separação de misturas?
Existem vários métodos de separação de misturas e a escolha de algum deles depende das características das substâncias misturadas.
Nos tópicos a seguir, iremos estudar cada um deles, mas agora veja quais são os fatores que influenciarão na escolha do método adequado:
- Tipo de mistura: homogênea ou heterogênea;
- Natureza dos elementos químicos que formam as misturas;
- Densidade, temperatura e solubilidade dos elementos.
Para facilitar o entendimento, agrupamos os métodos em duas categorias: os que servem para misturas homogêneas (destilação, evaporação, solidificação…) e os para misturas heterogêneas (catação, levigação, centrifugação, filtração, decantação…).
As técnicas podem se basear em princípios físicos ou químicos, pois usamos as propriedades dos componentes das misturas para separá-los. Essas propriedades podem ser o ponto de fusão, o ponto de ebulição, a solubilidade, a densidade, entre outros.
- Você é uma daquelas pessoas que tem fome de conhecimento? Então siga o Beduka no Instagram para conteúdos diários.
Como separar uma mistura homogênea? Exemplos!
Para misturas homogêneas, aquelas que possuem uma única fase e que é formada por substâncias miscíveis, é mais comum se utilizar os seguintes processos:
Destilação simples
A destilação simples é o processo de separação que envolve substâncias sólidas e líquidas. O princípio utilizado é o ponto de ebulição. A mistura é aquecida até uma das substâncias evaporar e a outra restar no recipiente.
É possível canalizar o vapor para um condensador e recuperar o que evaporou em forma de líquido.
Exemplo:
Se pegarmos uma amostra de água do mar e aquecermos essa mistura até ela ebulir (criar borbulhas), veremos que restará apenas sal no fundo do recipiente.
Isso acontece porque a temperatura de ebulição da água é bem mais baixa que a do sal. Assim, as moléculas de água são induzidas a evaporar, mas as de sal não.
Destilação fracionada
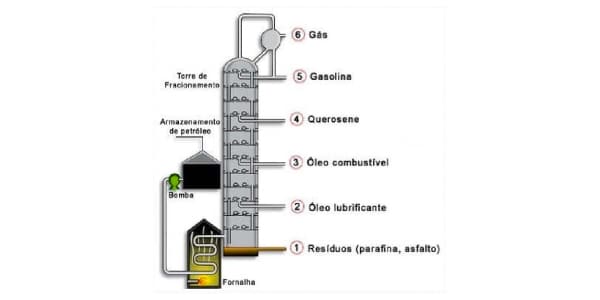
A destilação fracionada costuma ser aplicada em misturas formadas por 2 ou mais líquidos e usa o princípio do ponto de ebulição para aquecê-la e separá-la.
A novidade nesse processo é que ele possui um aparelho cheio de níveis que atingem diferentes pontos de ebulição por vez. Assim, é possível separar várias substâncias diferentes em um mesmo processo.
Normalmente, o produto desejado é o que possui o ponto de ebulição mais alto, mas os produtos secundários (que foram formados no meio do caminho) podem ter outras aplicações.
Exemplo:
A produção dos derivados de petróleo sempre passa pela destilação fracionada. O petróleo é aquecido e o vapor passa por diversos “pratos”, sendo que cada um coleta um composto derivado dependendo da sua temperatura de ebulição.
Vaporização
A vaporização, também conhecida por evaporação, é um processo mais natural e demorado. Nele, apenas deixamos a mistura em repouso até a parte líquida evaporar. Então, restará o soluto na forma sólida.
Observe que o componente líquido é perdido para a atmosfera, pois não envolve nenhuma aparelhagem artificial que possa fazer a água evaporada condensar e ser recuperada.
Exemplo: na realidade, a produção de sal marinho é feita pela evaporação porque é mais barato que a ebulição!
Destilação por arraste
Esse método utiliza o calor do vapor de água e é ele quem vai passar por uma mistura e fazer algum de seus componentes evaporar junto.
Exemplo:
Se colocamos folhas de eucalipto sobre a saída de vapor quente da sauna, logo o ar fica “refrescante”. Isso ocorre porque o calor do vapor “arrasta” consigo uma determinada substância da folha.
Liquefação fracionada
A liquefação fracionada costuma ser aplicada em gases e consiste em resfriar a mistura de forma gradual até os gases tornarem-se líquidos. Após isso, passam pela destilação fracionada e são separados conforme os seus pontos de ebulição.
Exemplo: separação dos componentes do ar atmosférico.
Fusão fracionada
A fusão fracionada costuma ser aplicada em misturas formadas apenas por sólidos de diferentes pontos de fusão. A mistura é aquecida até atingir o menor ponto de fusão, então um dos sólidos irá se liquefazer. Depois, basta passar por um filtro ou peneira e teremos as duas substâncias separadas.
Exemplo: separação dos componentes do ouro 18 quilates.
Solidificação fracionada
A solidificação fracionada se aplica a líquidos miscíveis com diferentes pontos de fusão. A diferença aqui é que iremos fazer o resfriamento deles. Assim, a temperatura é diminuída até o menor ponto de fusão e apenas um dos componentes é transformado em sólido.
Exemplo: separar a parafina dos resíduos do petróleo.
Como separar uma mistura heterogênea? (Exemplos)
Para misturas heterogêneas, aquelas que possuem duas ou mais fases, é mais comum se utilizar os seguintes processos:
Catação
Na catação, separamos os sólidos usando a propriedade de tamanhos diferentes. Também é possível fazer isso quando se trata de um sólido em um líquido, visto que é para misturas heterogêneas.
Podemos usar recursos como as mãos, uma pinça, um pegador, etc.
Exemplo: catar pedras dentre os grãos de feijão.
Levigação
A levigação é usada para separar sólidos que possuem diferentes densidades. Isso é feito quando fazemos a água correr por entre os sólidos e o menos denso é levado pela corrente enquanto o mais denso fica onde está.
Exemplo: separar o cascalho do ouro. Muito usado pelos garimpeiros à beira do rio.
Ventilação
A ventilação também é usada para separar sólidos que possuem diferentes densidades, mas isso é feito utilizando uma rajada de ar. Quando o vento passa, leva consigo a substância menos densa.
Exemplo: soprar para separar a casca do amendoim.
Filtração
A filtração é o método que usamos para separar substâncias sólidas de gases ou sólidas não dissolvidas em líquidos. Para isso, um filtro retém o componente sólido de uma mistura.
Exemplo: coar café ou usar a água do filtro de casa.
Existe uma modalidade chamada filtração à vácuo, em que a velocidade da filtração é acelerada. Isto ocorre porque o líquido filtrado não apresenta a resistência do ar ao cair dentro do recipiente. Exemplo: separar areia da água ou uma mistura pastosa.
Decantação

A decantação é um processo que acontece naturalmente e com o tempo, utilizado a diferença de densidades. Pode ser observado entre dois líquidos não miscíveis ou entre um sólido não dissolvido em líquido.
Naturalmente o componente menos denso da mistura é posicionado em cima do componente mais denso, devido a ação da gravidade.
Exemplo: separar água de óleo ou água de areia.
Centrifugação
A centrifugação é um método que acelera o fenômeno da decantação por meio de movimentos circulares. Isso acontece quando a mistura é colocada na centrífuga, um aparelho que rotaciona e acelera a translação dos componentes.
Exemplos: máquina de lavar retira excesso de água da roupa ou no laboratório para separar os elementos do sangue.
Separação magnética
Como o próprio nome aponta, esse método precisa de um ímã para retirar o componente metálico ferromagnético que está em meio a uma mistura de sólidos.
Exemplo: separar a limalha de ferro da areia.
Atenção: nem todos os metais são magnéticos (atraídos por imã), tome cuidado com as pegadinhas!
Flotação
Na flotação um líquido é adicionado a uma mistura formada por dois sólidos de diferentes densidades. Assim, quando estiverem em meio líquido, um irá flutuar (menos denso) e o outro não (mais denso). Depois, basta fazer uma decantação e filtração.
Exemplo: adicionar água em uma mistura formada por areia e isopor.
Sifonação
A sifonação é um método no qual usamos mangueira, pipeta, canudo, seringa ou qualquer objeto do tipo. Isso é feito para retirar o líquido mais denso ou menos denso de uma mistura formada por apenas líquidos.
Exemplo: Separar os componentes da mistura formada por água e óleo.
Coagulação e Floculação
A coagulação é um método no qual uma substância é adicionada a uma mistura para que ela se una aos componentes sólidos que estejam em suspensão em um líquido. Essa substância irá “atrair” quimicamente os sólidos e aglomera-los na superfície.
Exemplo: adicionar sulfato de alumínio na água em uma estação de tratamento de água.
A floculação é um método que complementa a coagulação, já que nele a mistura é agitada para favorecer a ação do coagulante.
Tamisação ou Peneiração

A peneiração é o método em que usamos uma peneira para separar os sólidos de tamanhos diferentes.
Exemplo: peneirar uma mistura de farinha e arroz para separar os grãos.
Dissolução fracionada
A dissolução é o método no qual um líquido é adicionado a uma mistura formada por dois sólidos com o objetivo de dissolver apenas um deles. Depois que um dos sólidos estiver diluído na parte líquida, basta aplicar qualquer método para separar líquidos de sólidos.
Exemplo: adicionar água em uma mistura formada por sal e areia e depois realizar filtração ou decantação.
Gostou do nosso artigo sobre a separação de misturas? Confira outros artigos do nosso blog e se prepare para o Enem da melhor maneira! Você também pode se organizar com o nosso plano de estudos, o mais completo da internet, e o melhor: totalmente gratuito!
Queremos te ajudar a encontrar a FACULDADE IDEAL! Logo abaixo, faça uma pesquisa por curso e cidade que te mostraremos todas as faculdades que podem te atender. Informamos a nota de corte, valor de mensalidade, nota do MEC, avaliação dos alunos, modalidades de ensino e muito mais.
Experimente agora!





